11/30(土)快晴○
11月最後の日は青空の広がる好天になりました。
各中学の先陣を切って中島中の3年生は内申点が告知されました。満足いく内申点だった人もいれば、納得いかない点数だった人もいる事と思います。
内申点が出て学調の結果も出ると,学校の進路指導のカードが出そろう事になります。不安があったら、学校面談の前でも後でも構わないので文理にお電話ください。
現状の正確な分析。面談で言われそうなこと。言われたことの補足をして、納得の上に頑張れるよう知恵を絞ります。
文理を頼って下さい!
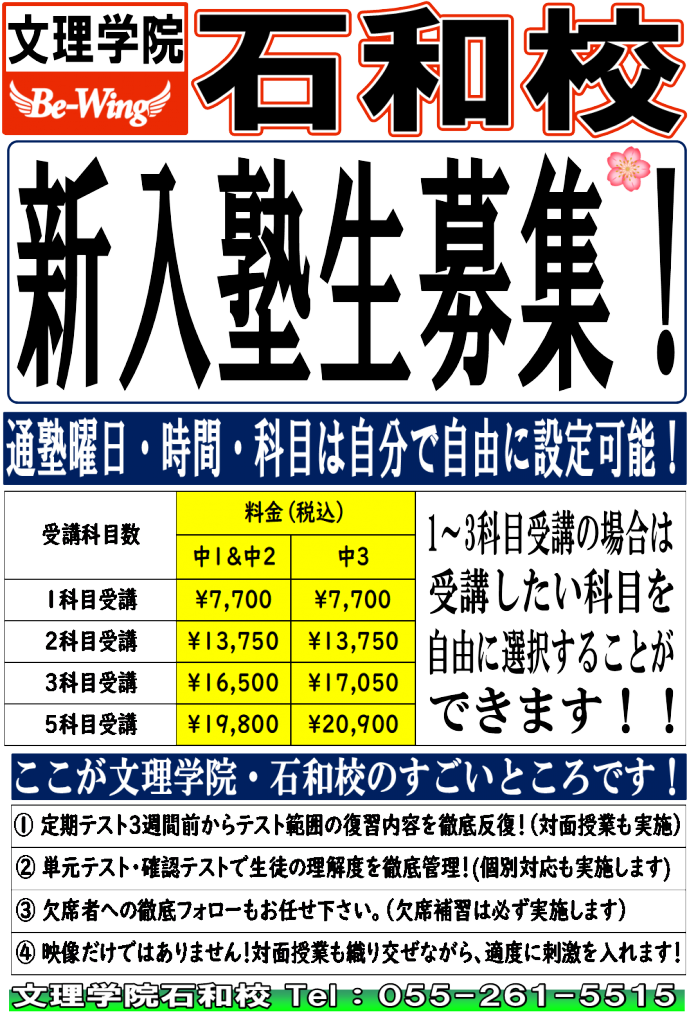
来週投函される校舎チラシを作成しました。

昨日は前から気になっていた丸子のお店で食事

エビフライがスタンドで立てて提供されました。
マイナンバーカードの更新のため、藤枝市役所に行きました。久々に市役所に寄ってみたら、さすがサッカーの町藤枝。サッカーミュージアムが併設されていました。
【建物と展示入り口。キャプテン翼の高橋陽一先生のキャラが描かれていました】


【展示品の数々。地元出身の現代表コーチの長谷部さん。名波さん。藤枝東出身の中山雅史選手関連の物が多く展示されていました】










狭いスペースながら、サッカーの町と言う自負を感じる掲示でした。
⛄冬期講習生受付中❅[タップすると中原校冬期講習概要が開きます]
この冬は文理学院の冬期講習で熱くなろう!!
❆☃冬期講習説明会③☃❅


日時:12月7日(土)午後6:00~6:45
持ち物:筆記用具・スリッパ
お電話いただければ平日に個別での説明をいたします。お申込・お問い合わせは下記文理学院中原校にお電話ください
文理学院中原校☎054-204-6755
【中原校は昨年度高校入試合格率100%!】






































 甲府南西校 神戸先生 理科
甲府南西校 神戸先生 理科

 大里校 由井先生 理科
大里校 由井先生 理科 今回は高等部の堀内先生による授業もありました!
今回は高等部の堀内先生による授業もありました! 生徒の皆さん、10コマ連続の授業本当におつかれさまでした!
生徒の皆さん、10コマ連続の授業本当におつかれさまでした!

